Itrakonazola kapsula 100 mgir plaša spektra -pretsēnīšu zāles, kas pieder triazola atvasinājumu klasei. Tās darbības galvenais mehānisms ir inhibēt ergosterola, kas ir sēnīšu šūnu membrānu galvenā sastāvdaļa, sintēzi, izjaucot šūnu membrānas integritāti un caurlaidību, izraisot sēnīšu šūnu satura noplūdi un nāvi.
Formulācijas optimizācija
Molekulmasa ir 705,64, un tās kapsulas forma ir iesaiņota cietā želatīna kapsulas apvalkā, kas satur baltas vai gaiši dzeltenas tabletes formas daļiņas. Palīgvielas ir hidroksipropilmetilceluloze, polietilēnglikols 20000, titāna dioksīds un FD&C zilās/sarkanās krāsvielas, lai nodrošinātu zāļu stabilitāti un vizuālo atpazīšanu. Lai uzlabotu biopieejamību, kapsulas jālieto uzreiz pēc ēšanas. Šajā laikā kuņģa skābes sekrēcija var veicināt zāļu izšķīšanu, palielinot uzsūkšanās ātrumu līdz 55% (absorbcijas ātrums tukšā dūšā ir mazāks par 30%).


Papildu informācija par ķīmisko savienojumu:
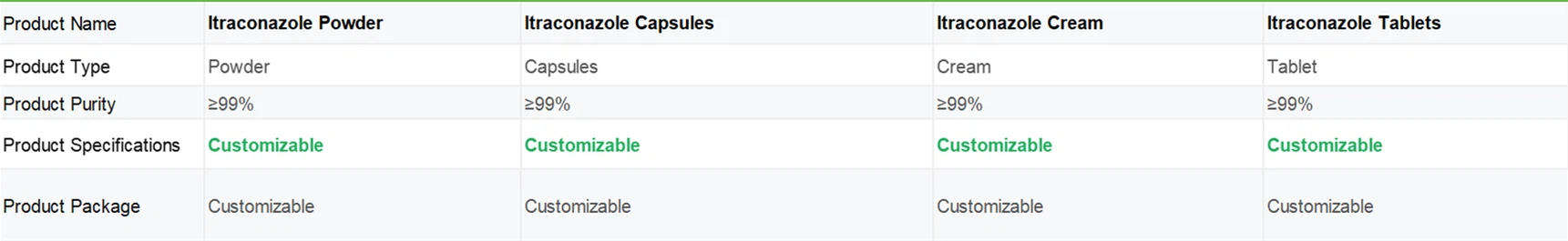
Mūsu produkta forma


Itrakonazola +. COA


Kā triazola plaša spektra{0}}pretsēnīšu zāļu pārstāvis,itrakonazola kapsula 100 mgpanākt efektīvu pretsēnīšu darbību, izmantojot vairāku{0}}mērķu sinerģisku darbību. Šīs zāles veido daudzslāņu antibakteriālu barjeru, kavējot sēnīšu šūnu membrānu galveno komponentu sintēzi, traucējot enerģijas metabolismu, izjaucot šūnu sienas integritāti un regulējot saimniekorganisma imūnās atbildes.
1.1 Precīza sterīnu sintēzes ceļa bloķēšana
Sēnīšu šūnu membrānu stabilitāte ir atkarīga no specifiskās ergosterola klātbūtnes, un tā sintēzes process ietver lanosterola pārvēršanu par ergosterolu. Itrakonazols bloķē lanosterīna pārvēršanos par 14 - demetilētu lanosterīnu, ar augstu afinitāti saistoties ar citohroma P450 atkarīgo 14 - demetilāzi (CYP51). Šis solis ir ātrumu ierobežojošais solis ergosterola biosintēzē. Zāļu iedarbība izraisa patoloģisku lanosterīna uzkrāšanos šūnu membrānā, savukārt ergosterola prekursora 24 metilēndihidrolanosterīna uzkrāšanās vēl vairāk traucē membrānas plūstamību.


1.2. Šūnu membrānas struktūras un funkcijas dubulta iznīcināšana
Ergosterola trūkums izraisa būtiskas izmaiņas šūnu membrānas caurlaidībā
Samazināta membrānas plūstamība: pavājinās mijiedarbība starp ergosterola un fosfolipīdu molekulām, izraisot patoloģisku membrānu proteīnu sadalījumu
Materiālu transportēšanas traucējumi: no ATP atkarīga jonu sūkņa funkcija ir traucēta, palielināta intracelulārā kālija jonu izplūde
Membrānas integritātes sabrukums: elektronu mikroskopijas novērojumi liecina par ievērojamu Candida albicans šūnu membrānas vezikulāciju pēc 24 stundu ilgas ārstēšanas
Šis strukturālais bojājums tieši izraisa sēnīšu šūnu satura noplūdi. Klīniskie pētījumi ir parādījuši, ka itrakonazola minimālā inhibējošā koncentrācija (MIK) ir 0,01–0,5 μg/ml Candida un 0,25–2 μg/ml Aspergillus gadījumā, parādot tā spēcīgo antibakteriālo aktivitāti.
2.1. Šūnu sieniņu sintēzes kavēšana
Itrakonazols inhibē - glikāna, kas ir galvenā šūnu sienas sastāvdaļa, šķērssaistēmu, samazinot -1,3-glikāna sintāzes gēna (FKS1) ekspresiju. Skenējošās elektronu mikroskopijas novērojums parādīja, ka pēc 72 stundu ilgas apstrādes Aspergillus fumigatus šūnu sieniņā parādījās acīmredzamas poras, un pektīna saturs samazinājās par 40% -60%. Šis efekts veido sinerģisku efektu ar ehinokandīniem, nodrošinot teorētisko pamatu kombinētai terapijai.
2.2. Enerģijas vielmaiņas traucējumi
Zāles inhibē mitohondriju elpošanas ķēdes kompleksu III un bloķē ATP sintēzi:
Samazināts skābekļa patēriņa līmenis: Candida albicans samazināja skābekļa patēriņu par 65%
ATP līmenis samazinās: intracelulārā ATP koncentrācija samazinās no normālās vērtības 3,2 mmol/g līdz 0,8 mmol/g


Metabolisma vidējā tilpuma uzkrāšanās: dzintarskābe, citronskābes cikla starpprodukts, uzkrājas līdz pat trīs reizēm par normālo līmeni
Šī vielmaiņas kavēšana izraisa sēnīšu augšanas apstāšanos G1 fāzē un šūnu dalīšanās indeksa samazināšanos par vairāk nekā 80%.
2.3. Bioplēves veidošanās bloķēšana
Itrakonazols var kavēt Candida albicans bioplēves veidošanā iesaistīto galveno gēnu, piemēram, ALS3 un HWP1, ekspresiju.
Bioplēves biezuma samazināšana: lāzera konfokālās mikroskopijas mērījums parāda biezuma samazināšanos no 120 μm līdz 35 μm
Ekstracelulārās matricas samazināšana: polisaharīdu saturs samazināts par 70%
Uzlabota zāļu iekļūšana: Zāļu koncentrācija bioplēvē palielinās 4-6 reizes
Šī īpašība padara to par īpašu terapeitisku vērtību ar ugunsizturīgu katetru{0}}saistītām infekcijām.
3.1. Rakstu atpazīšanas receptoru aktivizēšana
Itrakonazols var pārregulēt Toll līdzīgu receptoru (TLR) 2/4 ekspresiju un uzlabot makrofāgu atpazīšanas spēju pret - glikānu. Eksperiments parādīja, ka pēc ārstēšanas ar zālēm makrofāgu fagocītiskais indekss palielinājās no 1,2 līdz 3,8, un reaktīvo skābekļa sugu (ROS) ražošana palielinājās 2,5 reizes.
3.2. Citokīnu regulēšana
Inhibējot IL-10 sekrēciju, vienlaikus veicinot IL-12 un TNF izdalīšanos, zāles var mainīt Th2 tipa imūnsistēmu. Kriptokoku meningīta modelī itrakonazola terapijas grupā IFN līmenis cerebrospinālajā šķidrumā palielinājās piecas reizes, salīdzinot ar kontroles grupu, un fugālā klīrenss palielinājās par 60%.


3.3. Neitrofilu funkcijas uzlabošana
Zāles var uzlabot neitrofilu spēju veidot ārpusšūnu slazdus (NET):
Palielināta DNS izdalīšanās: plūsmas citometrijas analīze parādīja, ka NET pozitīvo šūnu īpatsvars palielinājās no 15% līdz 42%.
Paaugstināta histonu baktericīdā aktivitāte: Histons H2A trīs reizes palielina Aspergillus baktericīdo efektivitāti
Šis imunitāti uzlabojošais efekts ir īpaši svarīgs pacientiem ar novājinātu imunitāti, jo tas var samazināt izplatīto infekciju sastopamību.

Kā plaša spektra{0}}triazola pretsēnīšu zāles,itrakonazola kapsula 100 mgir plaši izmantots klīniskajā praksē, taču tā iekšķīgi lietojamajiem preparātiem (piemēram, kapsulām) joprojām ir problēmas, piemēram, lielas biopieejamības svārstības, nevienmērīgs mērķa orgānu sadalījums un zāļu -rezistento celmu efektivitātes samazināšanās. Lai uzlabotu efektivitāti, samazinātu toksicitāti un aizkavētu zāļu rezistences attīstību, nākotnē ir nepieciešami sasniegumi formulēšanas jauninājumu, molekulārās modifikācijas un imūnsinerģiskās terapijas jomā. Balstoties uz zāļu formas īpašībām, tiks sniegts sistemātisks izklāsts par tās turpmākajiem pētniecības virzieniem.
Nanoformulācijas attīstība: izkļūšana caur perorālo absorbcijas barjeru
Tradicionālajām itrakonazola kapsulām ir zema zāļu šķīdība un ievērojama pirmā loka iedarbība, kā rezultātā biopieejamība ir tikai aptuveni 55% (tukšā dūšā) līdz 65% (pēc lielas-tauku diētas), ar ievērojamām individuālām atšķirībām. Nanotehnoloģijas var būtiski uzlabot zāļu perorālās uzsūkšanās efektivitāti, regulējot to daļiņu izmēru un virsmas īpašības.
1. Cietās lipīdu nanodaļiņas (SLN)
SLN izmanto cietos lipīdus (piemēram, monoglicerīdus) kā nesējus, lai itrakonazolu iekapsulētu lipīdu kodolos, izmantojot augsta spiediena homogenizācijas vai mikroemulsifikācijas metodes. Tās priekšrocības ietver:
Biopieejamības uzlabošana:
Liposomas var veicināt zāļu uzsūkšanos caur zarnu limfātisko sistēmu, apiet pirmo aknu darbību un palielināt biopieejamību līdz vairāk nekā 80% (apstiprināts eksperimentos ar dzīvniekiem).
01
Kontrolēt zāļu izdalīšanos:
Pielāgojot lipīdu kušanas temperatūru (piemēram, izmantojot jauktus lipīdus) un daļiņu izmēru (100-300 nm), var panākt 12-24 stundu ilgstošu izdalīšanos, samazinot zāļu koncentrācijas svārstības asinīs.
02
Uzlabota stabilitāte:
Cietie lipīdi var aizsargāt zāles no kuņģa skābes un enzīmu noārdīšanās, padarot tās piemērotas pacientiem ar nepietiekamu kuņģa skābes sekrēciju vai kuriem nepieciešama ilgstoša{0}}ārstēšana.
03
Izaicinājums:
Optimizējiet lipīdu materiālus, lai izvairītos no kristalizācijas izraisītas zāļu eksplozijas izdalīšanās, un risiniet jautājumu par daļiņu izmēru viendabīgumu liela mēroga{0}}ražošanā.
04
2. Dendrimers polimēru nesēji
Dendrītiskajiem polimēriem (piemēram, PAMAM) ir ļoti sazarotas struktūras un virsmas funkcionālās grupas, kuras var ķīmiski modificēt, lai panāktu mērķtiecīgu piegādi:
Mērķtiecīga piegāde uz zarnām:
B12 vitamīna vai folijskābes savienošana uz polimēru virsmas var veicināt zāļu uzsūkšanos caur zarnu epitēlija šūnām, izmantojot receptoru{1}}mediētu endocitozi.
01
Iekļūst sēnīšu bioplēvē:
Dendrīta struktūra var iznīcināt bioplēves ekstracelulāro matricu, uzlabojot zāļu caurlaidību dziļām sēnīšu infekcijām, piemēram, invazīvu plaušu aspergilozi.
02
Vairāku zāļu kopīga ielāde:
Tās iekšējais dobums var vienlaikus iekapsulēt itrakonazolu un pastiprinātājus (piemēram, vorikonazolu), aizkavējot zāļu rezistences attīstību sinerģiskas iedarbības dēļ.
03
Izaicinājums:
Nesēja toksicitātes un zāļu slodzes līdzsvarošana un tā vielmaiņas drošuma pārbaude cilvēka organismā.
04
Strukturālās optimizācijas izpēte: precīza modifikācija pret zālēm{0}}rezistentām baktērijām
Zāļu -rezistentu sēņu (piemēram, pret azolu rezistentu Candida) mērķa enzīmu CYP51 (piemēram, Y132F, G448S) mutācijas izraisa itrakonazola saistīšanās afinitātes samazināšanos. Zāļu aktivitātes uzlabošana vai farmakokinētisko īpašību uzlabošana, izmantojot ķīmiskas modifikācijas, ir galvenais, lai pārvarētu zāļu rezistenci.
1. Fluorētu atvasinājumu sintēze
Fluora atomu ievadīšana itrakonazola molekulās var mainīt to elektronu sadalījumu un lipīdu šķīdību, tādējādi uzlabojot to antibakteriālo aktivitāti
Mehānisma optimizācija:
Fluora atomi var uzlabot hidrofobo mijiedarbību starp zālēm un CYP51 aktīvajām vietām, pārvarot mērķa enzīmu mutācijas zāļu rezistentās baktērijās.
01
Antibakteriālā spektra paplašināšana:
Fluorēti atvasinājumi samazina ne Candida albicans (piemēram, Candida albicans un Candida krusei) MIC vērtību 2–4 reizes, vienlaikus saglabājot to inhibējošo iedarbību uz Aspergillus.
02
Uzlabota vielmaiņas stabilitāte:
Fluora atomi var samazināt zāļu oksidatīvo metabolismu aknās, pagarināt pusperiodu līdz vairāk nekā 24 stundām un samazināt ievadīšanas biežumu.
03
Izaicinājums:
Ir nepieciešams optimizēt fluora atoma ievadīšanas vietu (piemēram, triazola gredzenu vai sānu ķēdi), izmantojot augstas{0}}caurlaidības skrīningu, lai izvairītos no aktivitātes zuduma vai paaugstinātas toksicitātes.
04
2. Prekursoru dizains
Priekšzāles ķīmiski modificējot maskē zāļu polārās grupas, uzlabojot tā šķīdību ūdenī un membrānas caurlaidību, vienlaikus atbrīvojot aktīvās sastāvdaļas pēc fermentatīvās hidrolīzes in vivo:
Ūdens šķīdības uzlabošana:
Piemēram, saistīšanaitrakonazola kapsula 100 mgar dzintarskābes anhidrīdu, lai iegūtu sukcināta priekšzāles, var palielināt tā šķīdību ūdenī 50 reizes, padarot vieglāku iekšķīgi lietojamu šķīdumu vai sausu suspensiju sagatavošanu.
01
nzarnu specifiskā aktivācija:
Izveidojiet savienojuma saites, kas ir jutīgas pret zarnu esterāzēm, ļaujot priekšzālēm izdalīt zāles galvenokārt resnajā zarnā un samazinot kuņģa skābes bojājumus zālēm.
02
Zāļu rezistences maiņa:
Priekšzāles var apiet pret zālēm{0}}rezistento baktēriju (piemēram, Cdr1, Mdr1) izplūdes sūkņus un atjaunot zāļu uzkrāšanās koncentrāciju šūnās.
03
Izaicinājums:
Ir nepieciešams līdzsvarot priekšzāļu stabilitāti un fermentatīvās hidrolīzes ātrumu un pārbaudīt tā efektivitāti sarežģītos infekcijas modeļos.
04
Kombinētā imūnterapija: aktivizē saimnieka aizsardzības mehānismus
Tradicionālā pretsēnīšu terapija balstās uz zālēm, kas tieši iznīcina baktērijas, savukārt imūnterapija uzlabo saimniekorganisma imūnreakciju, nodrošinot ilgtermiņa{0}}aizsardzību un samazinot atkārtošanās risku. Itrakonazola un imūnterapijas kombinācijai ir sinerģiskas uzlabošanas potenciāls.
1. Kombinācijā ar PD-1 inhibitoriem
PD-1 ir inhibējošs receptors uz T šūnu virsmas, un tā ekspresiju var regulēt sēnīšu infekcijas, lai izvairītos no imūnās uzraudzības.
Mehānisma sinerģija:
PD-1 inhibitori (piemēram, pembrolizumabs) var bloķēt PD-1 saistīšanos ar ligandu (PD-L1), atjaunojot T šūnu atpazīšanu un iznīcinot spēju pret fugāļu antigēniem.
Uzlabota terapeitiskā iedarbība:
Eksperimenti ar dzīvniekiem ir parādījuši, ka itrakonazola un PD-1 inhibitoru kombinācija var ievērojami samazināt invazīvās kandidozes mirstības līmeni un samazināt sēnīšu slodzi plaušās.
Drošības priekšrocības:
Perorāla lietošana var ierobežot sistēmisko imūnsistēmas aktivāciju un samazināt autoimūno slimību risku.
Izaicinājums:
Ir nepieciešams optimizēt zāļu ievadīšanas laiku un devu (piemēram, agrīna infekcijas kombinētā terapija), lai izvairītos no citokīnu vētrām, ko izraisa pārmērīga imūnsistēmas aktivācija.
2. CAR-T šūnu terapija
Himērisko antigēnu receptoru T šūnas (CAR-T) ir ģenētiski modificētas, lai ekspresētu receptorus, kas vērsti pret sēnīšu antigēniem, panākot specifisku nogalināšanu:
Mērķa atlase:
Karstuma šoka proteīns 90 (Hsp90) ir galvenā molekula fugāļu izdzīvošanai, un tas ir vāji ekspresēts saimniekšūnās, padarot to par ideālu mērķi.
Pastāvīgs uzlabojums:
Ieviešot atmiņas T šūnu epitopus, CAR{0}}T šūnas var palikt organismā ilgu laiku, nodrošinot ilgstošu aizsardzību.
Indikāciju paplašinājums:
Papildus invazīvām sēnīšu slimībām CAR-T terapiju var izmantot arī hronisku sēnīšu infekciju (piemēram, hroniskas plaušu aspergilozes) uzturošai ārstēšanai.
Izaicinājums:
Jārisina fugālo antigēnu imunogenitāte un jāoptimizē CAR-T šūnu amplifikācijas un reinfūzijas process (piemēram, jāizstrādā universāls CAR-T).
Itrakonazola kapsulu turpmākajai attīstībai ir nepieciešama nanotehnoloģiju, ķīmisko modifikāciju un imūnterapijas integrācija, lai izveidotu integrētu ārstēšanas sistēmu "zāļu nesēja saimnieks". Nanoformulācijas var uzlabot perorālās uzsūkšanās efektivitāti, strukturālā optimizācija var pārvarēt zāļu rezistenci, un imūnterapija var aktivizēt saimniekorganisma aizsardzības mehānismus. Nākotnē ir nepieciešama starpdisciplināra sadarbība (piemēram, materiālzinātnē, sintētiskajā ķīmijā, imunoloģijā), lai paātrinātu laboratorijas rezultātu pārņemšanu klīniskajā praksē, galu galā panākot pretsēnīšu terapijas precizitāti, personalizēšanu un ilgtermiņa efektivitāti. Piemēram, sagaidāms, ka SLN iekapsulētu flukonazola priekšzāļu kapsulu izstrāde kopā ar PD-1 inhibitoriem pret zālēm rezistentu invazīvu sēnīšu slimību ārstēšanai kļūs par standarta protokolu nākamās paaudzes pretsēnīšu ārstēšanai.
Itrakonazola kapsula 100 mgieņem nozīmīgu vietu pretsēnīšu terapijas jomā, izmantojot vairāku{0}}līmeņu un daudzmērķu antibakteriālo mehānismu. Tās darbības mehānisms ietver vairākus aspektus, piemēram, šūnu membrānas traucējumus, vielmaiņas traucējumus un imūno regulējumu, kas atspoguļo gan pašas zāles molekulārās īpašības, gan cieši saistītas ar saimnieka imūno stāvokli. Padziļinot izpratni par zāļu rezistences mehānismiem un zāļu mijiedarbību, kā arī nepārtraukti attīstot jaunas formulēšanas tehnoloģijas, itrakonazola klīniskā pielietošana kļūs precīzāka un efektīvāka, nodrošinot spēcīgāku ieroci sēnīšu infekciju ārstēšanā.
Bieži uzdotie jautājumi
Kādas ir itrakonazola sastāvdaļas?
+
-
Kapsulas satur 100 mg itrakonazola, kas pārklāts ar cukura lodītēm. Neaktīvās sastāvdaļas ir cietā želatīna kapsula, hipromeloze, polietilēnglikols (PEG) 20 000, ciete, saharoze, titāna dioksīds, FD&C zilais Nr.. 1, FD&C zilais Nr.. 2, D&C sarkanais Nr.
Vai itrakonazols ir labs ādai?
+
-
Itrakonazolu dažreiz lieto iekaisīgām ādas slimībām, piemēram, atopiskai ekzēmai, seborejas dermatītam vai psoriāzei, ja tiek uzskatīts, ka sēnīte vai rauga sēnīte veicina stāvokli.
Kāds ir itrakonazola darbības mehānisms?
+
-
Itrakonazols veicina tā pretsēnīšu aktivitāti, inhibējot 14 -demetilāzi, sēnīšu citohroma P450 enzīmu, kas pārvērš lanosterolu par ergosterolu, kas ir svarīga sēnīšu šūnu membrānu sastāvdaļa.
Kāpēc lieto itrakonazolu?
+
-
Itrakonazola kapsulu lieto, lai ārstētu sēnīšu infekcijas, piemēram, aspergilozi (sēnīšu infekciju plaušās), blastomikozi (Gilkrista slimību) vai histoplazmozi (Dārlinga slimību). Sporanox® kapsulu lieto arī onikohimikozes (roku vai kāju nagu sēnīšu infekcijas) ārstēšanai.
Kāda ir itrakonazola dabiska alternatīva?
+
-
Redīsu EO ir spēcīga pretsēnīšu iedarbība pret itrakonazolu{0}}izturīgām Candida sugām, pat vairāk nekā itrakonazolam. Dažu EO pretsēnīšu iedarbību var palielināt, izmantojot zemas koncentrācijas.
Populāri tagi: itrakonazola kapsula 100 mg, piegādātāji, ražotāji, rūpnīca, vairumtirdzniecība, pirkt, cena, vairumā, pārdošanai