Shaanxi BLOOM Tech Co., Ltd. ir viens no pieredzējušākajiem acetaldehīda šķīduma cas 75-07-0 ražotājiem un piegādātājiem Ķīnā. Laipni lūdzam vairumtirdzniecībā augstas kvalitātes acetaldehīda šķīdumā cas 75-07-0, kas tiek pārdots šeit no mūsu rūpnīcas. Ir pieejams labs serviss un saprātīga cena.
Acetaldehīda šķīdums, pazīstams arī kā acetaldehīds, ir organisks savienojums, CAS 75-07-0, ķīmiskā formula ir CH3CHO. Pieder aldehīda ketonu organiskajiem savienojumiem, tas ir bezkrāsains un caurspīdīgs šķidrums ar asu smaržu, gaistošām un uzliesmojošām īpašībām. Tas viegli šķīst ūdenī un jebkurā proporcijā var tikt sajaukts ar organiskiem šķīdinātājiem, piemēram, etanolu, ēteri, benzolu, benzīnu, toluolu utt. To galvenokārt izmanto kā reducētāju, fungicīdu un standarta šķīdumu aldehīdu kolorimetriskai noteikšanai. Izmanto rūpniecībā acetaldehīda, etiķskābes, sintētiskā kaučuka u.c. ražošanai.
Plaši izmanto kā izejvielas, dezinfekcijas līdzekļus, sprāgstvielas, reducētājus etiķskābes, etiķskābes anhidrīda, butanola, poliacetaldehīda, sintētiskā kaučuka un citu produktu organiskai sintēzei, kā arī var izmantot, lai sagatavotu standarta šķīdumus formaldehīda noteikšanai ar kolorimetrisko metodi. Acetaldehīda rūpnieciskā ražošana ietver tādas metodes kā tieša etilēna oksidēšana, etanola oksidēšana, tieša acetilēna hidratācija, etanola dehidrogenēšana un etiķskābes hidrogenēšana. Tās pakārtotie produkti ir piridīns, krotonaldehīds un sorbīnskābe.

|
Ķīmiskā formula |
C2H4O |
|
Precīza Mise |
44 |
|
Molekulmasa |
44 |
|
m/z |
44 (100.0%), 45 (2.2%) |
|
Elementu analīze |
C, 54.53; H, 9.15; O, 36.32 |
|
|
|

1. Acetaldehīda katalītiskā oksidēšana
![]()
2. Acetaldehīda sadedzināšana

3. Sudraba spoguļa reakcija
![]()
4. Acetaldehīds un no jauna pagatavots vara hidroksīds

5. Acetaldehīds reaģē ar ūdeņradi, veidojot etanolu

Acetaldehīda šķīdumsvar ražot dažādos veidos:
1. Etilēna tiešās oksidēšanas metode Etilēns un skābeklis tiek tieši oksidēti, lai vienā solī sintezētu neapstrādātu acetaldehīdu caur katalizatoru, kas satur pallādija hlorīdu, vara hlorīdu, sālsskābi un ūdeni, un pēc tam gatavo produktu iegūst destilējot.
2. Etanola oksidēšanas metode Acetaldehīds tika iegūts ar etanola tvaiku oksidatīvo dehidrogenēšanu gaisā 300-480 grādu temperatūrā, par katalizatoru izmantojot sudraba, vara vai sudraba vara sakausējuma sietu vai daļiņas.
3. Acetilēna tiešās hidratācijas metode Acetilēns un ūdens tiek tieši hidratēti dzīvsudraba katalizatora vai bezdzīvsudraba katalizatora iedarbībā, lai iegūtu acetaldehīdu. Dzīvsudraba bojājumu problēmas dēļ tas pakāpeniski ir aizstāts ar citām metodēm.
4. Etanola dehidrogenēšanas metode vara katalizatora klātbūtnē ar kobaltu, hromu, cinku vai citiem savienojumiem, etanolu dehidrogenē, lai iegūtu acetaldehīdu.
5. Piesātināto ogļūdeņražu oksidēšanas metode. Izejvielu patēriņa kvota: 610kg 99% acetilēna uz tonnu produkta, kas saražots ar acetilēna hidratāciju; Etanola oksidēšanas metode patērē 1200kg 95% etanola; Etilēna oksidēšanas metode (viena posma metode) patērē 710 kg 99% etilēna un 300 m3 skābekļa (99%). Komerciālais rūpnieciskais acetaldehīds, acetaldehīda tīrība ar etilēna metodi ir 99,7%, un acetaldehīda tīrība ar etanola metodi ir 98%.


Acetaldehīda šķīdumsir bezkrāsains, caurspīdīgs un gaistošs šķidrums ar asu smaku. Aldehīda grupa (- CHO) savā molekulārajā struktūrā nodrošina tai augstu reaktivitāti un var piedalīties dažādās ķīmiskās reakcijās. To plaši izmanto ķīmijas, farmācijas, pārtikas, ikdienas ķīmijas, lauksaimniecības un citās jomās.
Galvenās lietošanas jomas: ķīmiskie starpprodukti un šķīdinātāji

Etiķskābes un acetāta ražošana
Tā ir galvenā etiķskābes (CH3 COOH) rūpnieciskā izejviela, kas oksidācijas reakcijās (piemēram, ar Wacker metodi) pārvērš acetaldehīdu etiķskābē un tālāk sintezē atvasinājumus, piemēram, vinilacetātu un etiķskābes anhidrīdu. Etiķskābi izmanto kā skābes regulatoru tekstilizstrādājumu apdrukā un krāsošanā, lai uzlabotu audumu krāsošanas efektu; Kā skābuma regulētājs pārtikas rūpniecībā to plaši izmanto garšvielu un konservētu pārtikas produktu ražošanā. Vinilacetāts ir galvenā izejviela celulozes acetāta (piemēram, plēves substrātu un plastmasas) ražošanai, un acetaldehīdam ir galvenā savienojošā loma šajā procesā.
Pentaeritritola sintēze
Sārmainos apstākļos acetaldehīds kondensējas ar trim formaldehīda molekulām, veidojot pentaeritritolu (C (CH ₂ OH) ₄), svarīgu poliolu, ko izmanto sveķu, pārklājumu, smērvielu un sprāgstvielu (piemēram, pentaeritritola tetranitrāta) ražošanā. Pentaeritritola atvasinājumi ir neaizstājami tādās jomās kā kosmosa un elektroniskais iepakojums. Acetaldehīds kā reakcijas sākumpunkts tieši nosaka rūpnieciskās ķēdes pagarinājuma virzienu.


Piridīna un tā atvasinājumu sagatavošana
Katalizatora iedarbībā tas reaģē ar amonjaku, veidojot piridīnu, ko tālāk var izmantot B3 vitamīna (niacīna), prettuberkulozes zāļu izoniazīda uc sintezēšanai. Piridīna savienojumi ieņem galveno vietu farmācijas, pesticīdu un krāsvielu rūpniecībā. Piemēram, piridīns reaģē ar hloretiķskābi, sintezējot herbicīdu 2,4-D, un acetaldehīda līdzdalība padara iespējamu šo augstas pievienotās vērtības produktu sintēzi.
Šķīdinātājs un tīrīšanas līdzeklis
Tas var izšķīdināt sveķus, eļļas un dažādas organiskas vielas, un to parasti izmanto metāla tīrīšanai, elektronisko komponentu attaukošanai un precīzai instrumentu dekontaminācijai. Pusvadītāju ražošanā acetaldehīdu izmanto, lai notīrītu atlikušo fotorezistu uz silīcija plātņu virsmas. Tā zemās virsmas spraiguma īpašības var iekļūt mikrometru līmeņa spraugās, nodrošinot tīrību, kas atbilst nanometru līmeņa standartiem. Lai gan dažas lietojumprogrammas ir aizstātas toksicitātes problēmu dēļ, joprojām ir grūti tās pilnībā nomainīt augstas-precīzas tīrīšanas gadījumos.

Īpašs mērķis: farmācijas un pārtikas rūpniecība

Farmaceitisko starpproduktu sintēze
Antibiotikas un pretvīrusu zāles: tās piedalās antibiotiku, piemēram, penicilīna un cefalosporīnu, sānu ķēžu struktūru sintēzē un ievada specifiskas funkcionālās grupas, izmantojot aldola kondensācijas reakcijas, lai uzlabotu zāļu aktivitāti. Piemēram, pēc kondensācijas un hidrolīzes ar cianīda joniem un amonjaku vielu var izmantot alanīna sintezēšanai, ko tālāk var izmantot pretepilepsijas līdzekļa gabapentīna sintezēšanai.
Vitamīnu ražošana: Acetaldehīds ir svarīgs izejmateriāls B ₁ vitamīna (tiamīna) sintēzei, kas kondensējas ar ciānetiķskābi, veidojot tiazola gredzenu un galu galā B ₁ vitamīna molekulas. Turklāt acetaldehīdu izmanto arī kā starpproduktu A vitamīna, - jonona sintēzei, un tā reakcijas selektivitāte tieši ietekmē A vitamīna iznākumu.
Anestēzijas līdzekļi un miegazāles: tās tiek hlorētas, veidojot trihloracetaldehīdu, un to hidrāts (hlorālhidrāts) ir plaši izmantots kā sedatīvs hipnotisks līdzeklis. Lai gan blakusparādību dēļ tas ir aizstāts ar drošākām alternatīvām, tam joprojām ir pielietojums veterinārmedicīnas jomā.


Pārtikas piedevas un esence
Garšvielas: Nelielos daudzumos šīs vielas dabiski ir kafijā, maizē un nogatavojušos augļos, piešķirot tiem īpašu aromātu. Rūpniecībā acetaldehīdu izmanto, lai pagatavotu augļu esenci, piemēram, apelsīnus, apelsīnus un ābolus, un vīna esenci, piemēram, vīnu un rumu. Acetaldehīda koncentrācija galīgajā aromatizētajā pārtikā ir aptuveni 3,9–270 mg/kg.
Konservanti: var kavēt mikrobu augšanu un pagarināt pārtikas glabāšanas laiku. Piemēram, siera ražošanā acetaldehīdu izmanto, lai novērstu pelējuma piesārņojumu, vienlaikus uzlabojot siera garšu.
Deinonilēšanas process: to kādreiz izmantoja kafijas deinterkalācijai, ekstrahējot kofeīnu un destilējot, lai atgūtu šķīdinātāju. Lai gan superkritiskā CO2 ekstrakcijas tehnoloģija pakāpeniski ir kļuvusi populāra, dažos reģionos tās process joprojām tiek saglabāts.
Piedevas ikdienas ķīmiskajiem produktiem
Šampūns un dušas želeja: kā smērvielas tie var uzlabot produktu tekstūru, padarot matus mīkstus un ādu gludu. Tā zemā nepastāvība nodrošina stabilitāti produkta uzglabāšanas laikā, kā arī piedalās esences lēnās atbrīvošanās sistēmā, lai pagarinātu smaržas saglabāšanas laiku.
Kosmētika: Acetaldehīdu izmanto, lai sintezētu noteiktus antioksidantus, novērstu eļļas oksidēšanos un sasmakšanu preparātos un pagarinātu produkta glabāšanas laiku. Turklāt tā atvasinājumi (piemēram, glioksilskābe) tiek izmantoti kā balinošās sastāvdaļas ādas kopšanas līdzekļos, samazinot melanīna ražošanu, inhibējot tirozināzes aktivitāti.


(1) Sp2 hibridizācija
Gan aldehīdu, gan ketonu struktūras satur oglekļa skābekļa dubultsaites (- C=O, karbonilgrupa). Oglekļa atoms veido trīs sp2 hibridizētas orbitāles ar skābekļa atomu un diviem citiem atomiem, veidojot trīs sigma saites, kas atrodas vienā plaknē ar aptuveni 120 grādu saites leņķi. Atlikusī karboniloglekļa p orbitāle, kas nepiedalās hibridizācijā, no sāniem pārklājas ar vienu skābekļa atoma p orbitāli, veidojot π saiti, savukārt abās skābekļa atoma p orbitālēs ir divi vientuļo elektronu pāru pāri.
Kā piemēru ņemot formaldehīdu, kuram ir visvienkāršākā struktūra, oglekļa skābekļa dubultsaites un oglekļa ūdeņraža vienkāršās saites garums ir attiecīgi 120,3 µm un 110 µm.

Tā kā skābekļa atomiem ir lielāka elektronegativitāte salīdzinājumā ar oglekļa atomiem, elektronu mākonis oglekļa skābekļa dubultsaitē mēdz būt novirzīts pret skābekļa atomiem, kā rezultātā ap tiem ir lielāks elektronu mākoņu blīvums, savukārt oglekļa atomu elektronu mākoņu blīvums ir mazāks. Tāpēc karbonilgrupām ir polaritāte unAcetaldehīda šķīdumsir polāra molekula, kas arī izskaidro, kāpēc acetaldehīds viegli šķīst polāros šķīdinātājos (līdzīga šķīdība).
(2) Alfa ūdeņraža atoms
① Vāji skābs
Aldehīdu un ketonu alfa ūdeņraža atomi ir ļoti aktīvi divu galveno iemeslu dēļ: pirmkārt, karbonilgrupu elektronu izņemšanas indukcijas efekts; Otrais ir alfa oglekļa ūdeņraža saišu hiperkonjugācijas efekts uz karbonilgrupām.

Ņemot par piemēru 2-metilcikloheksanonu, izotopu apmaiņas eksperimenti ir parādījuši, ka alfa ūdeņraža atomam blakus karbonilgrupai ir augsta aktivitāte un to var aizstāt ar deitērija atomiem deuterētā nātrija oksīda (smagais nātrija hidroksīds, NaOD) un smagā ūdens (D2O) iedarbībā.

Lai gan dažādu karbonilsavienojumu alfa H aktivitāte atšķiras, aldehīdiem ir spēcīgāks skābums, salīdzinot ar vienas sērijas alkāniem, alkīniem un ketoniem. No vienas puses, alkilgrupu steriskais šķērslis ir lielāks nekā ūdeņraža atomiem, un, no otras puses, hiperkonjugācijas efekts starp alkilgrupām un karbonilgrupām samazina karbonilgrupu pozitīvo lādiņu.

Piezīme: p ir negatīvs logaritms, un jo mazāks pKa, jo spēcīgāks ir skābums.
② Tautomerisms
Parasti lielākajai daļai aldehīdu un ketonu ir tautomēri. Ņemot par piemēru acetaldehīdu, starp ketona un enola formām ir tautomēri. Enola formas struktūras nestabilitātes dēļ acetaldehīda ketona formas struktūra veido gandrīz 100%, ar līdzsvara konstanti aptuveni 6,0 × 10-5.

Piezīme: Enola struktūras nestabilitātes iemesls ir tas, ka oglekļa oglekļa dubultsaišu klātbūtne palielina oglekļa atoma π elektronu mākoņa blīvumu. Tomēr skābekļa spēcīgās elektronegativitātes dēļ elektronu mākonim ir tendence tuvoties skābekļa atomam. Šis pretrunīgais rezultāts izraisa enola struktūras nestabilitāti.
③ Aldola kondensāts
Atšķaidīta sārma šķīduma iedarbībā acetaldehīda molekulās var notikt aldola kondensācijas reakcija zemā temperatūrā, kur - ūdeņraža atomi uzbrūk karbonilskābekļa atomiem, bet citas funkcionālās grupas savienojas ar karboniloglekļa atomiem, veidojot - hidroksibutiraldehīdu, kas dubulto oglekļa atomu skaitu.

(3) Nukleofīlā pievienošana
Oglekļa atoma pozitīvajam lādiņam karbonilgrupā viegli uzbrūk nukleofili, un skābā un sārmainā vidē tas var tikt pakļauts π - saites šķelšanās pievienošanas reakcijai.

① Ciānūdeņražskābe
Ciānūdeņražskābe ir tipisks nukleofils, kas reaģē arAcetaldehīda šķīdumslai iegūtu 2-hidroksipropionitrilu (- hidroksinitrilu). Reakcijas ātrums tiks ievērojami paātrināts sārmainos apstākļos, jo HCN kā vāja skābe sārmainos apstākļos var radīt cianīda negatīvos jonus (CN-), tādējādi palielinot reaģentu koncentrāciju; Gluži pretēji, ja to veic skābos apstākļos, ūdeņraža joni tiek protonēti ar karbonilgrupām, pastiprinot karboniloglekļa elektrofilitāti, kas neveicina reakcijas gaitu un palēnina reakcijas ātrumu.

HCN + NaOH → NaCN + H2O
CH3CHO + HCN → CH3-CH(OH)-CN

Turklāt 2-hidroksipropionitrilu var hidrolizēt skābos apstākļos, lai iegūtu 2-hidroksipropionskābi (pazīstama kā "pienskābe"). Tāpēc ūdeņraža cianīda nukleofīlo pievienošanas reakciju var izmantot, lai sintezētu hidroksi skābes ar papildu oglekļa atomu.
CH3-CH(OH)-CN + 2H2O + H+ → CH3-CH(OH)-COOH + NH4+
② Nātrija bisulfīts
Acetaldehīds un piesātināta nātrija bisulfīta šķīduma pārpalikums var tikt pakļauts nukleofīlai reakcijai, veidojot nātrija bisulfīta aduktus bez nepieciešamības izmantot katalizatoru.
CH3CHO + NaHSO3 → CH3-CH(OH)-SO3Na
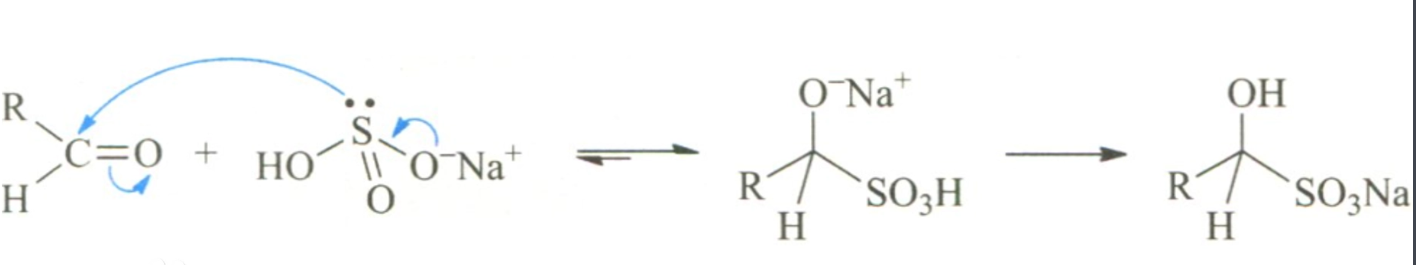
Nātrija bisulfīta adukts (nātrija alfa hidroksisulfonāts) viegli šķīst ūdenī, bet grūti izšķīst organiskajos šķīdinātājos, tāpēc tas izkliedējas no organiskās fāzes uz ūdens fāzi, veidojot kristālus. Tāpēc šo reakciju var izmantot, lai atdalītu aldehīdus no organiskiem savienojumiem, kas nešķīst ūdenī.
Piezīme: Nātrija alfa hidroksisulfonāts reaģē ar nātrija cianīdu, un sulfonskābes grupu var aizstāt ar cianīda grupu, veidojot alfa hidroksinitrilu (nitrila spirtu), tādējādi izvairoties no ļoti toksiska un gaistoša ūdeņraža cianīda veidošanās.
CH3-CH(OH)-SO3Na + NaCN → CH3-CH(OH)-CN + Na2SO3
③ Formatējiet reaģentu
Acetaldehīds var reaģēt ar Grignar reaģentu (pazīstams kā "Grignard reagent", saīsināts kā "RMgX") bezūdens ētera klātbūtnē, vispirms radot magnija aizvietotus savienojumus (starpproduktus) un pēc tam hidrolizējot skābos apstākļos, lai tieši radītu spirtus. Šī reakcija ir arī viens no veidiem, kā sintezēt spirtus, izmantojot nukleofīlas pievienošanas reakcijas, līdzīgi kā organiskie litija reaģenti.

Kā piemēru ņemot cikloheksāna reakciju uz ogļūdeņraža bāzes reaģentu ar acetaldehīdu.
CH3CHO + C6H11-MgX → H11C6-CH(OH)-CH3

Piezīme: Formātu reaģentu 1901. gadā sintezēja franču zinātnieks Fransuā Ogists Viktors Grignārs (1871-1935). Tas ir organisks magnija reaģents, kas veidojas, reaģējot organiskiem halogēna (hlora, broma, joda) savienojumiem (halogenētie alkāni, aktīvi halogenētie aromātiskie ogļūdeņraži) ar magnija ēteri sausā ūdenī.
④ Alkohols
Spirtiem ir arī afinitāte, un skābju, piemēram, p-toluolsulfonskābes un hlorūdeņraža katalīzes rezultātā tie var iziet nukleofīlas pievienošanās reakcijas ar acetaldehīdu, veidojot nestabilus pusacetālus, kurus pēc tam var noņemt no vienas ūdens molekulas, veidojot acetālus.

Specifiskais reakcijas mehānisms ir šāds: pirmkārt, karbonil joni un ūdeņraža joni tiek pakļauti protonēšanai, veidojot oksonija jonus, kas palielina karboniloglekļa atoma elektrofilitāti; Otrkārt, pievienošanas reakcijās ar spirtiem tiek zaudēti protoni, kā rezultātā veidojas nestabili pusacetāli; Pēc tam tas savienojas ar H+, veidojot oksonija jonus dehidratācijai; Visbeidzot, tas reaģē ar spirtu, veidojot stabilāku aldehīdu, un kopējais rezultāts ir tāds, ka viena aldehīda ketona molekula var reaģēt ar divām spirta molekulām, veidojot vienu aldehīda molekulu.

Ņemot par piemēru metanolu, tas var reaģēt ar acetaldehīdu, veidojot dimetoksietānu (aldehīdu).
CH3CHO + 2CH3OH → (H3CO)2-CH-CH3 + H2O
⑤ Ūdens
Skābā vidē ūdenī var notikt nukleofīlas pievienošanās reakcijas ar acetaldehīdu, veidojot dihidroksietānu (diolu).

CH3CHO + H2O → (HO)2-CH-CH3
Piezīme: divu ar vienu oglekļa atomu savienotu hidroksilgrupu molekulārajai struktūrai trūkst termodinamiskās stabilitātes, un pēc dehidratācijas tai ir tendence atgriezties aldehīdos un ketonos, norādot, ka pievienošanas reakcija starp ūdeni un karbonilu ir atgriezeniska reakcija ar līdzsvaru, kas ir novirzīts uz reaģenta pusi.
⑥ Amonjaks un tā atvasinājumi
Visi aldehīdi un ketoni var tikt pakļauti nukleofīlai pievienošanas reakcijai ar amonjaku un tā atvasinājumiem (piemēram, hidroksilamīnu, hidrazīnu, fenilhidrazīnu, semikarbazīdu utt.), kas rada stabilus produktus, piemēram, oksīmu, hidrazonu, fenilhidrazonu un urīnvielu. Tomēr produkti, kas iegūti reakcijā ar amonjaku, ir nestabili.

Ņemot par piemēru 2,4-dinitrofenilhidrazīnu, attēlā ir parādīts ķīmiskais vienādojums reakcijai ar acetaldehīdu un dehidratāciju, lai iegūtu 2,4-dinitrofenilhidrazonu.

Piezīme. Oksīms, hidrazons un urīnviela parasti ir stabili kristāli ar fiksētu kušanas temperatūru. Hidrolīze skābā vidē var atjaunot karbonila struktūru. Tāpēc šīs nukleofīlās reakcijas var izmantot, lai identificētu un attīrītu aldehīdus un ketonus.
Dažu amīnu atvasinājumu produkti, kas reaģē ar karbonilgrupām

(4) Oksidācijas reakcija
① Krāsu reakcija
Aldehīdu grupaAcetaldehīda šķīdumsmolekulas var oksidēt līdz - COO - ar Fēlinga reaģentu un Tollensa reaģentu, radot attiecīgi ķieģeļsarkanas nogulsnes (Cu2O) un sudraba spoguli (elementu Ag). Aldozes (reducējošā cukura) noteikšanas princips slēpjas tajā, un reakcija, kas notiek ar Tollensa reaģentu (kurai nepieciešama karsēšana), ir pazīstama arī kā "sudraba spoguļa reakcija" [3].
CH3CHO + 2Ag(NH3)2OH → 2Ag↓+ 3NH3↑+ 2H2O + CH3COONH4
CH3CHO + 2Cu(OH)2 → Cu2O↓+ 2H2O + CH3COOH
Piezīme. Fēlinga reaģents un Tollensa reaģents ir reaģenti, kas var identificēt reducējošās vielas. Pirmo parasti veido nātrija hidroksīda (NaOH) un vara sulfāta (CuSO4) šķīdums, ko 1849. gadā izgudroja vācu ķīmiķis Hermans fon Fēlings (1812-1885); Pēdējo var pagatavot tikai in situ, un tā galvenā sastāvdaļa ir sudraba nitrāta amonjaka šķīdums, proti, Ag (NH3) OH, kas pazīstams arī kā "sudraba amonjaka šķīdums", ko 19. gadsimtā izgudroja vācu ķīmiķis Bernhards Tollens (1841-1918).
② Spēcīgs oksidētājs
Pateicoties aldehīdu grupu reducējamībai, tās var oksidēt līdz etiķskābei ar neorganisku spēcīgu oksidētāju kālija permanganātu. Skābos apstākļos kālija permanganāts tiek reducēts līdz divvērtīgiem mangāna joniem, kā rezultātā tumši purpursarkanais šķīdums izbalējis; Sārmainos apstākļos tas tiek samazināts līdz IV valentam mangāna dioksīdam, un parādība ir tāda, ka dziļi purpursarkanais šķīdums izbalē, veidojot brūngani melnas nogulsnes. Jonu vienādojums ir šāds.
5CH3CHO + 2MnO4- + 6H+ →2Mn2+ + 5CH3COOH +3H2O
3CH3CHO + 2MnO4- + H2O →2MnO2↓+ 3CH3COOH + 2OH-
Piezīme: Kālija permanganātam ir spēcīgākas oksidējošas īpašības skābā vidē, un tas tiek reducēts līdz zemākas valences savienojumiem. Līdzīgi spēcīgi oksidētāji ir kālija dihromāts (K2Cr2O7), hromskābe (H2CrO4), ūdeņraža peroksīds (H2O2) utt.
③ katalītiskā oksidēšana
Vara metāla katalīzes un karsēšanas apstākļos acetaldehīdu var oksidēt ar skābekli līdz etiķskābei. Pirmkārt, varš karsēšanas apstākļos reaģē ar skābekli, veidojot vara oksīdu, kas pēc tam darbojas kā oksidants un reaģē ar acetaldehīdu, lai reducētos par elementāru varu (katalizatoru) [2] [20-28].
2Cu + O2 → 2CuO
CH3CHO + CuO → Cu + CH3COOH
2CH3CHO + O2 → 2CH3COOH
④ Skābeklis (sadegšana)
Acetaldehīdu kā organisku savienojumu var sadedzināt skābeklī, lai iegūtu oglekļa dioksīdu un ūdeni (pilnīgi oksidētu).
2CH3CHO + 5O2 → 4CO2 + 4H2O
(5) Redukcijas reakcija
Acetaldehīds satur nepiesātinātās oglekļa skābekļa dubultsaites (- C=O), kuras ar reducēšanas aģentiem var reducēt līdz hidroksimetilgrupai (- CH2OH).
① Katalītiskā hidrogenēšana
Acetaldehīdu var reducēt līdz etanolam ar ūdeņraža gāzi, iedarbojoties ar metāla katalizatoriem, piemēram, niķeli un pallādiju.
CH3CHO + H2 → CH3CH2OH
② Metāla hidrīds
Acetaldehīdu var reducēt līdz etanolam ar metālu hidrīdiem (spēcīgiem reducētājiem), piemēram, litija alumīnija hidrīdu, nātrija borhidrīdu utt. bezūdens ētera apstākļos.
CH3CHO + LiAlH4 +2H2O → CH3CH2OH + LiAlO2 + 3H2↑
CH3CHO + NaBH4 + 3H2O → CH3CH2OH + NaBO3 + 4H2↑
③ Clemmensen restaurācija
HCl un cinka dzīvsudraba (Zn Hg) iedarbībā acetaldehīda aldehīdu grupu var reducēt līdz metilgrupai, tas ir, acetaldehīds tiek reducēts līdz etānam stipros skābos apstākļos. Šī reakcija ir piemērota karbonilsavienojumu reducēšanai, kas ir jutīgi pret sārmiem.

Hg nepiedalās Klemensena reducēšanas reakcijā, bet darbojas kā katalizators. Pēc dzīvsudraba amalgamas (Zn Hg) sakausējuma izveidošanas ar cinku cinka aktivitāte palielinās, jo sakausējumā veidojas elektrisks pāris, tādējādi veicinot reakciju.
Cinka amalgamu var pagatavot, reaģējot cinka pulveri/cinka daļiņas ar dzīvsudraba sāli (HgCl2) atšķaidītā sālsskābes šķīdumā. Elementārais cinks var reducēt divvērtīgos dzīvsudraba jonus līdz elementārajam dzīvsudrabam, un tad dzīvsudrabs veido dzīvsudraba amalgamu uz cinka virsmas, un reducēšanās reakcija notiek uz cinka aktivētās virsmas.
Piezīme: Klemensena reducēšanas reakciju 1913. gadā atklāja dāņu ķīmiķis Ēriks Kristians Klemensens (1876-1941).
④ Kishner Wolff Huang Minglong restaurācija
Aldehīdi un ketoni var reaģēt ar bezūdens hidrazīnu, veidojot hidrazonus (C=NNHR), kas pēc tam var tikt sadalīti slāpekļa gāzē, karsējot ar bezūdens etanolu un nātrija etoksīdu augstspiediena traukā līdz 180–200 grādiem. Sārmainos apstākļos karbonilgrupas tiek reducētas līdz metilēngrupām, un šo reakciju sauc par Volfa Kišnera reducēšanas reakciju.

Huang Minglong (1898-1979), slavenais organiskais ķīmiķis Ķīnā un CAS locekļa akadēmiķis, uzlaboja reakciju. Lielāku ražu var sasniegt, aizstājot bezūdens hidrazīnu ar hidrazīna ūdens šķīdumu. Tas ir, aldehīds vai ketons, nātrija hidroksīds, hidrazīna ūdens šķīdums un šķīdinātājs ar augstu viršanas temperatūru (dietilēnglikols, dietilēnglikols, HOCH2CH2OCH2CH2OH) tika kopīgi karsēti, veidojot hidrazonu, un pēc tam hidrazīna un ūdens pārpalikums tika iztvaicēts. Pēc hidrazona sadalīšanās temperatūras sasniegšanas reakcija tika uzkarsēta ar atteci līdz reakcijas beigām. Šo reakciju sauc par Wolff Kishner Huang Minglong reakciju.
Ņemot par piemēru acetaldehīdu, to var reducēt līdz etānam, izmantojot Wolff Kishner un Wolff Kishner Huang Minglong reakcijas, kas ir piemērotas skābju jutīgu karbonila savienojumu reducēšanai.
(6) Ūdeņraža saite
Acetaldehīds var veidot ūdeņraža saites ūdenī, kas ir vēl viens iemesls, kāpēc acetaldehīds (zemākie aldehīdi) viegli šķīst ūdenī.

FAQ
Kāda ir acetaldehīda smarža?
KĀ ACETALDEHĪDS SMARŽO VAI GARŠO? Tipiski sensorie deskriptori, kas saistīti ar acetaldehīdu, ir zaļie (Granny Smith) āboli, ķirbju mīkstums/sēklas, nenobriedis avokado un lateksa krāsa. Acetaldehīds šajā ziņā ir nedaudz unikāls; ka tā aromāta "raksturs" var mainīties, mainoties tā koncentrācijai.
Kāda ir acetaldehīda formula?
Acetaldehīds - C2H4O
Acetaldehīds, etanāls, ir bezkrāsains, ūdenī{0}}šķīstošs, degošs šķidrums, kura ķīmiskā formula ir C2H4O un strukturālā formula CH3CHO. Acetaldehīdam ir zema viršanas temperatūra 21 grādi.
Kādi dzērieni satur daudz acetaldehīda?
Turklāt acetaldehīdu satur tādi dzērieni kā tēja un bezalkoholiskie dzērieni (0,2–0,6 ppm), alus (0,6–24 ppm), vīns (0,7–290 ppm) un stiprie alkoholiskie dzērieni (0,5–104 ppm) 2).
Populāri tagi: acetaldehīda šķīdums cas 75-07-0, piegādātāji, ražotāji, rūpnīca, vairumtirdzniecība, pirkt, cena, lielapjoma, pārdošana









